Faites votre choix !
THÉORIE
Introduction
Atomes, molécules, ions
Électrons, protons, neutrons
Modèle de Bohr – atome d’hydrogène
Nombres quantiques
Mole
Oxydoréduction
Réactions des métaux et non-métaux
Diagramme de Lewis – Règles et Astuces
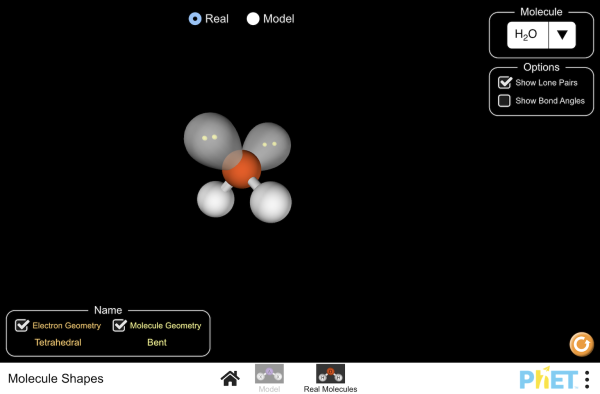
Simulateur de géométrie moléculaire
Polarité des molécules avec un atome central
Cycle énergétique de la liaison covalente
Cycle énergétique de la liaison ionique
Comment trouver les exercices ?
Quiz (réalisé par Langis Rouillard, Collège Ahuntsic)
Notation AXZ pour les atomes, Département de chimie, Cégep André-Laurendeau
Déterminer le nombre d’électrons contenus dans 2,10E5 ions SO42-
Déterminer le numéro atomique et le symbole d’un élément X sachant que 2,3E3 atomes de X contiennent 6,9E4 neutrons et qu’il correspond à : 55z X
Quel est le numéro atomique de l’élément X dans HXO42- sachant que 6,83E4 ions HXO42- contiennent 3,42E6 électrons ? Identifiez le symbole de l’élément X .
Z=15, P
Bonus !
Q3- Déterminez le numéro atomique et le symbole d’un élément X sachant que 2,3 x 103 atomes de X contiennent 1,403 x 105 neutrons et qu’il correspond à :
Rép : Z = 48, Cd
Corrigé : https://youtu.be/e-vD6vIlXH8
Modèle de Bohr
Du Modèle de Bohr (attention, l’Énergie est en électron-volt (eV)) au modèle de la mécanique quantique
Questions et solutions sur le modèle de Bohr
Page 15 : Quelle est la longueur d’onde de la 3e raie de Brackett ? Solution
Page 17 : 3 Questions sur les transitions électroniques Solution
Page 18 : Schémas des questions 5.17, 5.19, 5.20 et 5.24 Solution
Page 19 : Soit l’électron d’un atome d’hydrogène qui décrit initialement la 5e orbite de Bohr. Cet électron émet alors une radiation (un photon) de fréquence 6,9 x 1014 Hz. Solutions aux questions suivantes
a)Déterminez l’énergie du photon émis.
b)Déterminez la diminution d’énergie subie par l’électron à la suite de cette transition
c)Déterminez l’énergie de l’électron à la suite de cette transition
d)Déterminez le niveau n de l’électron suite à cette transition
e)Dans que domaine du spectre électromagnétique retrouve-t-on cette radiation émise ?
Correction de la page 28 (jpg)
Réponses de la page 38 (pdf)
La technique mole à mole :
version pdf (par Benoit Cromp)
Version vidéo (2011)
Exercices supplémentaires sur la mole :
Quelle est la masse de 4,20E-25 molécules d’eau ? 1.26E3 g d’H2O
Combien y a-t-il de mol.cules dans 7,05 g de H2O ? 2.355E23 molécules
Combien y a-t-il de moles d’atomes dans 0.0532 mol de SO4^(2-) ? 0.266 mol d’atomes
Combien y a-t-il d’atomes d’oxygène dans 0.0532 mol de SO4^(2-) ? 1.28E23 atomes
Déterminer la masse de H2O qui contient 2.85E24 protons ? 8,52 g d’H2O
Calculez le nombre d’ions SO4^(2-) qui contiennent 20.0 mol d’é ? 2,41E23 ions
Corrigé de l’exercice 2.21, du Chang
Réactions des métaux et non-métaux
revision_reactions_metaux_corrige
Diagramme de Lewis – Règles et Astuces
Simulateur de géométrie moléculaire
Polarité des molécules avec un atome central
Construction des modèles moléculaires : Tutoriels
Principe de base
Atome à 2 paquets d’électrons – BeH2
Atome à 3 paquets d’électrons – BH3
Atome à 4 paquets d’électrons –
Atome à 5 paquets d’électrons –
Double liaison – Liaison pi
Triple liaison – Liaison pi
Liaison de coordinence
Cycle énergétique de la liaison covalente
Cycle énergétique de la liaison ionique
NaCl : cycle énergétique
CaCl2 : cycle énergétique
LABORATOIRES
Laboratoire 1 : Chiffres significatifs (CS)
Lecture : Cahier de labo p 3 à 5
Cahier de labo p 123-132 Annexe 1 : IMPORTANT pour connaître les règles !!
Pratiquez : lecture d’échelle avec les exemples de la p 5.
CS dans les calculs avec les XR6 de la p 133 (réponse p 134)
N’oubliez pas de vous vêtir en accord avec les règles de sécurité au laboratoire. Apportez le cahier de laboratoire et le cahier Données et rapports.
À la fin du labo : remettre Cahier Données & Rapports, page 2
Rapport (3 jours ouvrables plus tard) : remettre Cahier Données & Rapports, pages 3 et 4 ET une feuille montrant un exemple de TOUS les calculs de la page 4.
Laboratoire 2 : Spectre visible de l’hydrogène
Lecture : Cahier de labo, p 7 à 15
Feuille de route individuelle obligatoire (sur 1 ou plusieurs feuilles mobiles, manuscrite seulement (pas à l’ordi):
- Nom
- But de l’expérience
- Matériel à sortir du tiroir (cette semaine : lunettes de sécurité seulement)
- Schéma du montage
- Manipulations sous forme de mots-clé, de dessins, d’organigramme (pas de copie du texte)
- Traitement des données : pas nécessaire !!!
voir un exemple feuille de route
N’oubliez pas de vous vêtir en accord avec les règles de sécurité au laboratoire. Apportez le cahier de laboratoire et le cahier Données et rapports.
À la fin du labo : remettre Cahier Données & Rapports, page 5
Rapport (3 jours ouvrables plus tard) : remettre Cahier Données & Rapports, pages 6 et 7 ET graphique
Laboratoire 3 : Analyse des cations
Lecture : Cahier de labo – Préparation en suivant les instructions de la page 101 (en haut).
Les pages 8 et 9 du cahier Données et rapports doivent être complétées avant le labo
La page 10 du cahier Données et rapports devra être remise en ENTRANT au labo.
Rapport à remettre sur place, alors faites une excellente préparation !
N’hésitez pas à venir me rencontrer si vous avez des questions.
Laboratoire 4 : Analyse des anions
Lecture : Cahier de labo – Préparation en suivant les instructions de la page 101 (en bas).
Les pages 12 et 13 du cahier Données et rapports doivent être complétées avant le labo
La page 14 du cahier Données et rapports devra être remise en ENTRANT au labo.
Rapport à remettre sur place, alors faites une excellente préparation !
N’hésitez pas à venir me rencontrer si vous avez des questions.
- Préparez bien votre feuille de route, car vous n’aurez pas le droit au texte du cahier de laboratoire.
- Indiquez bien les étapes de la partie D sur le diagramme d’analyse de la solution inconnue. Ce diagramme est primordial !! Annotez-le et utilisez-le en lab !
Laboratoire 5 : Décomposition quantitative d’un chlorate de potassium
Lecture : Cahier de labo – p 33-38 , Feuille de route standard
Laboratoire 6 : Technique d’utilisation de la pipette
Lecture : Cahier de labo – p 75-86
Feuille de route en 2 parties (2 paquets de feuille distincts) :
- Technique d’utilisation de la pipette (p 75-82) en 1 page recto-verso : mots-clés et/ou dessins
- Manipulations en 1 page (p84-85) : mots-clés et/ou dessins
Sarrau, vêtements adéquats, etc.
Remise de la page 49 de cahier de Données et Rapports, sur place, avant de partir.
Pas de rapport supplémentaire.
Laboratoire 7 : Modèles moléculaires 1
Préparation obligatoire à l’aide de la page 102 du cahier de laboratoire. Préparez les 3 molécules de Modèles Moléculaire I et l’ion.
Votre ligne : Selon votre numéro d’équipe + Le coéquipier a est le premier dans l’ordre alphabétique des noms de famille
Laboratoire 8 : Modèles moléculaires 2
Préparation obligatoire à l’aide de la page 102 du cahier de laboratoire. Préparez les 2 espèces de Modèles Moléculaire II.
Votre ligne : Selon votre numéro d’équipe + Le coéquipier a est le premier dans l’ordre alphabétique des noms de famille
Test Modèles moléculaires
Suivez les instructions suivantes : consignes pour les test modèles moléculaires
Préparez-vous en pratiquant au moins 2 lignes différentes de la vôtre sur la page 118 du cahier de laboratoire.
Laboratoire 9 : Métaux et non-métaux
Excellente révision pour le contrôle 3. Profitez-en.
Attention !!!! La préparation est longue et ne peut être réalisée à la dernière minute.
Toutes les instructions sont à la page 103 du cahier de labo.
Le rapport sera à remettre sur place, à la fin du labo.
Préparez-vous bien !!
N’hésitez pas à venir poser des questions si vous éprouvez des difficultés.
Laboratoire 10 : Stoechiométrie
Feuille de route standard
Remplir la page 46 du cahier de Données et Rapports avec les observations attendues et les équations et formules chimiques appropriées.
Devoir individuel Liaisons chimiques
Consultez l’annexe H p.119 du cahier de laboratoire
Vous devez vous pratiquer en utilisant les composés des pages 120 et 121. Choisissez votre ligne et au moins deux autres lignes très différentes de la vôtre.
Votre ligne : Selon votre numéro d’équipe+ Le coéquipier a est le premier dans l’ordre alphabétique des noms de famille